BAB 2
BENTUK MOLEKUL
A.Bentuk Molekul Berdasarkan Teori Tolsksn Pasang Elektron
Struktur lewis dari suatu molekul merupakan struktur yang dapat menggambarkan bagaimana posisi pasangan elektron yang mengelilingi atom pusat, baik pasangan elektron yang berikatan (PEI), maupun pasangan elektron yang tidak berikatan atau pasangan elektron bebas (PEB). Pasangan-pasangan ini elektron ini saling tolak-menolak. Ahli kimia mengemukakan bsuatu teori yang di kenal dengan nama teori VSEPR (Valence Shell Electron Repulsion).
Kelompok pasangan elektron dapat berupa ikatan tunggal, rangkap dua, dan ikatan rangkap tiga. Gambar brikut!
1.
- 2 ikatan tunggal 2. 2. 3 ikatan tunggal
Di dalam klasifikasi VSEPR ada beberapa huruf yang melambangkan atom pusat, atom yang mengelilingi atom pusat, dan elektron bebas, yaitu :
A = atom pusat
X = atom yang mengelilingi atom pusat
E = pasangan elektron bebas

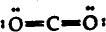
Tidak ada komentar:
Posting Komentar